Ágora dixital
En esta experiencia estudiaremos cómo se comportan los gases a partir del ampliamente reproducido, pero no siempre bien interpretado, experimento de la vela que se apaga.

Cesta de materiales
Presiona en los puntos interactivos de la imagen.
Manos a la obra
- Paso 1
-
- Se fijan las velas a la base del recipiente de vidrio. Para eso, se calienta, con un mechero, su base, aprovechando la cera generada como pegamento. Se coloca, en un extremo, una vela, y, en el otro, dos juntas.
- Paso 2
-
- Se añade agua del grifo en el recipiente de vidrio hasta, aproximadamente, la mitad de su volumen.
- Se puede añadir una gota de colorante alimentario para teñir el agua y hacer los resultados más visuales.
- Paso 3
-
- Se encienden las velas con el mechero. El resultado deberá de ser similar a lo que se muestra en la imagen:
Imaxe
- Paso 4
-
- Se colocan, de manera simultánea, los dos vasos sobre las velas, de manera que asienten en la base del recipiente de vidrio. Se observará que, a los pocos segundos, las velas se apagan, y el agua sube por el vaso hasta un punto, en el que se detiene.
- Paso 5
-
- Se repite el proceso, pero colocando, en vez de dos, tres velas juntas en un de los extremos del recipiente de vidrio que las contiene. Se observará algo similar a lo que ocurre en el punto 4, pero con una ligera diferencia (ver apartado 'Tips docentes').
- Paso 6
-
- Se analizan los resultados obtenidos en el punto 4 y en el punto 5.
- Paso 7
-
- Se puede realizar un experimento análogo, empleando velas con base de aluminio, en lugar de las empleadas en este experimento. Aquí, al no ser posible alterar el número de velas en un caso y en otro, se puede analizar lo que ocurre tapando una vela con un vaso caliente (se puede calentar, por ejemplo, con un mechero) y con un frío (se puede enfriar, por ejemplo, introduciéndolo en un recipiente con agua y hielo).
Tips docentes
INTRODUCCIÓN TEÓRICA
Presión y temperatura en los gases
La presión ejercida por un gas es el resultado de la colisión de las partículas que lo conforman contra las paredes del recipiente que lo contiene. Así, para una cierta masa de gas encerrada en un recipiente de paredes rígidas (volumen constante) la presión dependerá, de manera directamente proporcional, de la temperatura a la que se encuentre el gas. La temperatura es una medida de la energía cinética de las partículas del gas, por lo que, a más temperatura, mayor velocidad de desplazamiento tendrán. Esto hace que el número de colisiones contra las paredes del recipiente aumente, aumentando, también, su presión. La expresión matemática que relaciona la presión y la temperatura de un gas a volumen constante se conoce como la ley de Gay-Lussac, y tiene la siguiente forma:
p = k . T; donde p es la presión, en atm; k es una constante de proporcionalidad y T es la tempertura, en K.
Para ahondar en el entendimiento de cómo se comportan los gases, se puede emplear el siguiente laboratorio virtual PhET (https://phet.colorado.edu/sims/html/gas-properties/latest/gas-properties_all.html?locale=eres):
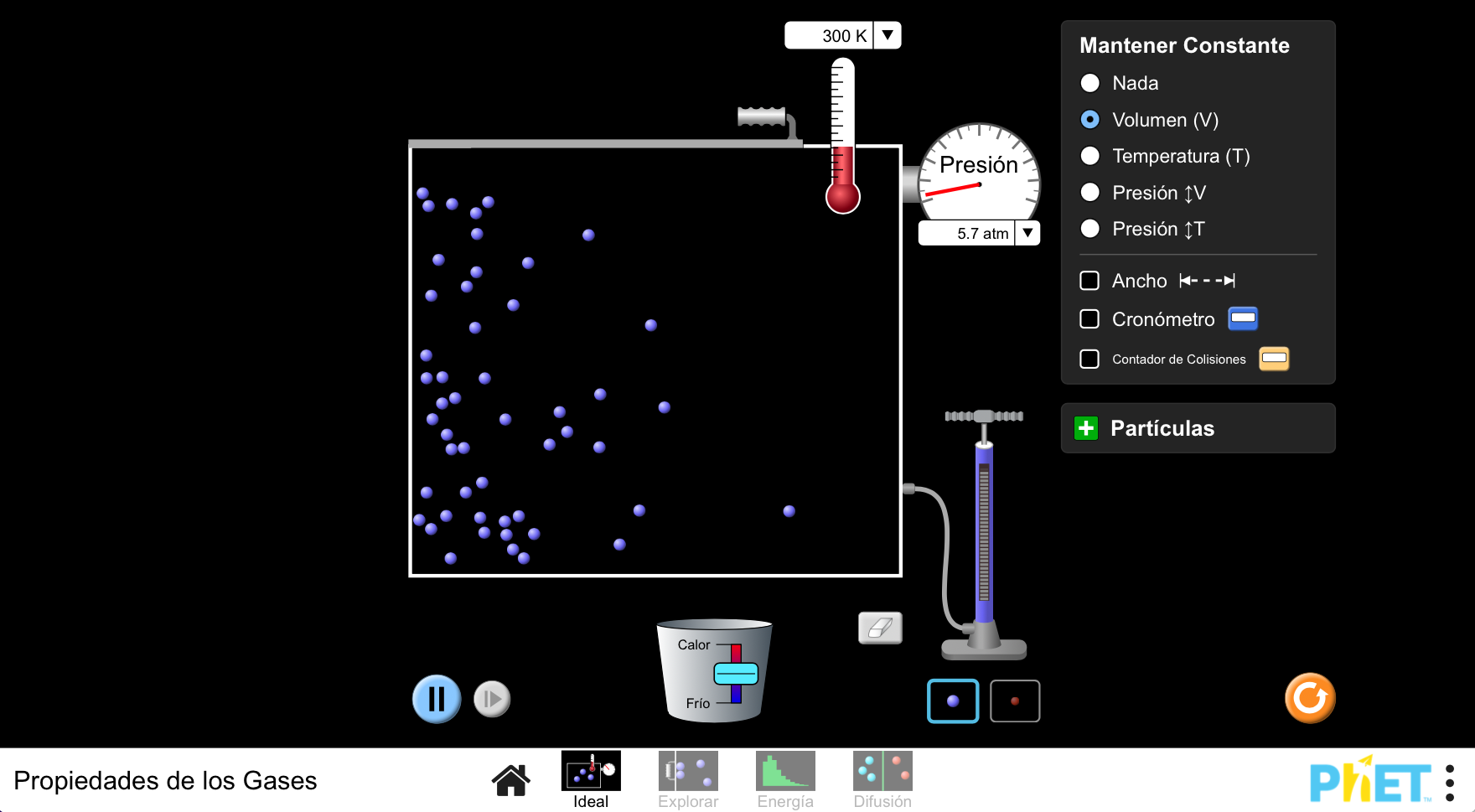
CONSEJOS METODOLÓGICOS Y TÉCNICOS
En este experimento, se tendrán en cuenta los siguientes puntos:
a) Entre un experimento y el siguiente, a no ser que se empleen velas nuevas, es importante secarlas bien, pues se mojan al ascender el agua por el vaso.
b) Entre un experimento y el siguiente, deberemos de secar el interior de los vasos con un poco de papel absorbente. Además, los agitaremos un par de veces, con el fin de renovar el aire contenido en su interior. De lo contrario, pueden almacenar un exceso de dióxido de carbono procedente de la combustión que provoque la extinción del fuego de las velas antes de lo que sería deseable.
c) No suele ocurrir si se fijan bien, pero si las velas se despegan de la base del recipiente de vidrio a medida que el agua asciende por el vaso, se puede emplear un poco de plastilina para fijarlas más firmemente.
d) Intentaremos tapar las velas de la manera más homogénea posible. La modificación de esta variable puede, especialmente en el caso de las velas con base de aluminio, alterar los resultados.
e) En el punto 4, se le puede plantear al alumnado que explique por qué se observa un ligero burbujeo cuando se tapan las velas con los vasos.
f) En el punto 5, el alumnado puede elaborar una hipótesis de los resultados esperados. Algunas cuestiones para guiar su elaboración pueden ser las siguientes: ¿qué pasa con el aire del vaso cuando tenemos tres velas, en lugar de dos, calentándolo? ¿El nivel del agua en el vaso será el mismo que en el punto anterior, superior o inferior? ¿Cabría esperar que el burbujeo al tapar las velas con el vaso fuera más intenso o menos intenso que en el punto 4?
ANÁLISIS DE LOS RESULTADOS OBTENIDOS
A menudo se emplea este experimento como una manera sencilla de determinar la cantidad de oxígeno en el aire. Así, suele indicarse lo siguiente:
i) Al tapar la vela con el vaso, el oxígeno se agota, pues se consume en la combustión, y la vela se apaga.
ii) Al agotarse el oxígeno, hay menos gas en el interior del vaso, ejerciendo, por lo tanto, una menor presión que el aire exterior.
iii) Se genera, así, una especie de vacío que hace que el agua ascienda por el vaso hasta que las presiones en el interior y en el exterior se igualan de nuevo.
iv) El agua que asciende por el vaso coincide exactamente con el volumen de oxígeno en el aire, pues es la única sustancia presente en el aire que se agota. Es importante tener en cuenta que en el proceso de combustión el oxígeno se consume, pero se producen otros gases, como dióxido de carbono y vapor de agua (que, finalmente, condensa), lo que invalida completamente la utilidad de este experimento para determinar el volumen de oxígeno en el aire.
Si todo lo expuesto fuera cierto, entonces en nuestro experimento obtendríamos el mismo resultado, independientemente del número de velas empleadas en cada caso, pues el volumen de aire (y, por lo tanto, de oxígeno) encerrado en el interior del vaso es exactamente el mismo. Si acaso, podríamos observar pequeñas variaciones (casi insignificantes) en el nivel del agua al modificar el número de velas, toda vez que el espacio ocupado por una vela no puede ser ocupado por el aire. Lo que se observa es lo siguiente:

Se ve perfectamente que el vaso con dos velas absorbe más agua que el que tiene sólo una. Esto se explica de la siguiente manera:
1. La presión de un gas aumenta al incrementar su temperatura, pues las partículas que lo conforman se mueven a mayor velocidad.
2. La presión del aire encerrado en el vaso de las dos velas será superior a la del aire encerrado en el vaso con sólo una.
3. La presión del aire encerrado en el interior de los vasos será superior a la atmosférica, pues está más caliente. Esto provoca que parte del aire del interior de los vasos "escape" del sistema y se observe un leve burbujeo cuando los vasos se sumergen en el agua. Resulta obvio que escapará un mayor volumen de aire cuanto más caliente esté, pues ejercerá una mayor presión. Así, disponemos de una menor masa de aire en el vaso con dos velas que en el vaso con una. Sin embargo, llega un punto en el que la presión externa e interna se igualan en los dos casos, por lo que no se observa, durante un muy breve instante de tiempo, ni burbujeo, ni absorción de agua por las paredes del vaso.
4. El CO2 producido en el proceso de combustión hace que la vela se apague, pues es un gas más denso que el oxígeno, y tenderá a quedar en las cercanías de la llama. El oxígeno no llega a agotarse por completo, tal y como demuestran diversos estudios (ver, por ejemplo, el trabajo The Persistence of the Candle-and-Cylinder Misconception, publicado en J. Chem. Ed. 1999, 76, 914).
5. Al apagarse la vela, desciende drásticamente la temperatura de la masa de gas contenida en el interior del vaso, lo que hace que su presión caiga, viéndose superada por la presión atmosférica (la presión ejercida por el aire externo sobre el agua), y que el vapor de agua condense (las paredes del vaso se empañan).
6. La caída de presión será más acusada en el vaso que tenga un mayor número de velas, pues perdió una mayor cantidad de aire en primera instancia, lo que provoca que el volumen de agua absorbido sea mayor.
En este punto, se repite el proceso, tal y como se indica en el punto 5 del procedimiento experimental, empleando tres velas juntas, en uno de los extremos del recipiente, en lugar de dos. Los resultados, al realizar el experimento, fueron los siguientes:

El volumen de agua en el vaso con tres velas es considerablemente superior a lo que se observa con una única vela, y al observado, también, en el vaso con dos velas, lo que está en consonancia con las explicaciones anteriores.
Hace falta destacar, no obstante, que lo indicado en los puntos anteriores son líneas generales, y que existen diversas situaciones intermedias que requerirían un análisis más detallado. Por ejemplo, cabría suponer, en base a lo expuesto, que el agua no debería de subir por el vaso hasta que la vela se apagara, algo que no es exactamente así. Esto puede explicarse toda vez que parte del vapor de agua condensa en las paredes del vaso antes de que la vela se apague, así como considerando que la energía cinética de las partículas del gas no es la suficiente para contrarrestar la presión atmosférica, entre otros aspectos.
Si se realiza el experimento con velas de base de aluminio, tal y como se indica en el punto 7 del apartado 'Manos a la obra', intentaremos que el diámetro de las velas y el de los vasos sea lo más ajustado posible, a fin de obtener unos resultados más claros. Si realizamos la experiencia tal y como se indica, obtendremos un nivel de agua claramente distinto en un vaso y en otro, tal y como se muestra en la imagen. La explicación es análoga a la del experimento comentado previamente.

Tu clase en un clic
Implementa esta microsecuencia en tu aula Moodle (Descarga disponible en gallego o castellano ).
|
Imaxe
 |
Imaxe
 |
